西安泰科迈医药承接的硝苯地平缓释片(Ⅱ)通过仿制药一致性评价
2021年05月12日
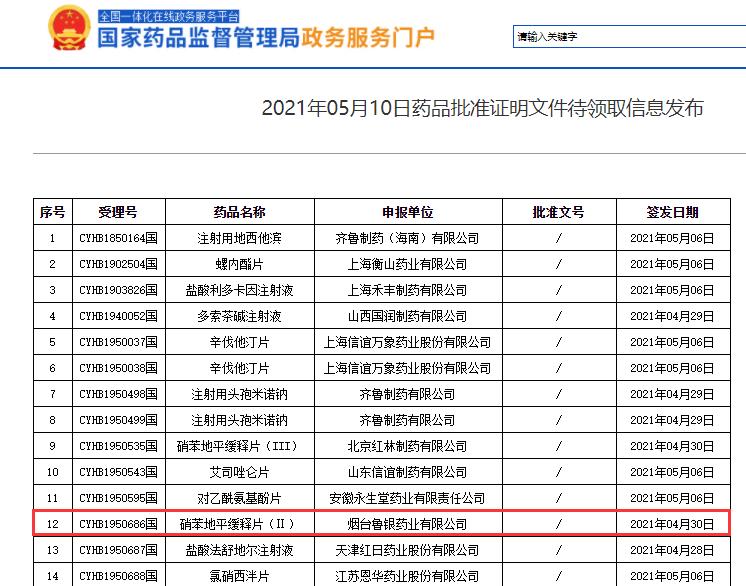
4月30日,烟台鲁银药业有限公司的硝苯地平缓释片(Ⅱ)仿制药质量和疗效一致性评价项目通过了国家药品监督管理局(NMPA)审批,取得了批件,这也是西安泰科迈医药科技股份有限公司承接的仿制药一致性评价技术委托项目的又一个成功典范。
硝苯地平缓释片(Ⅱ)主要治疗稳定型心绞痛(劳累型心绞痛)、血管痉挛型心绞痛和原发性高血压。原研公司为拜耳药品株式会社。中国上市的硝苯地平缓释片规格包含10mg、20mg、30mg,控释片规格包含60mg、30mg,缓释片20mg已经通过一致性评价的企业除了烟台鲁银药业外,还有上海信宜、青岛黄海、双鹤利民。10mg缓释片已经申报的企业为德州德药和扬子江江苏制药,目前暂未批准。
根据米内网数据显示,2019年硝苯地平缓释片(II)销售总额(终端价)为11.87亿元,其中企业排名前五分别是:青岛黄海制药有限责任公司47.99%,双鹤利民17.93%,烟台鲁银有限公司10.26%,迪沙药业10.05%,上海信宜天平有限公司5.86%。本次通过一致性评价后,可以助推鲁银药业稳固原有市场份额,进一步拓展市场空间。硝苯地平属于BCSII类药物,活性成分溶解性较差,故需要对API杂质、晶型(工艺前后、稳定性)、粒度(反向解析、粉碎方法、粒度控制)、避光等采取严格的措施。辅料、包装材料的选择进行了风险评估并制定了严格的内控标准,制剂研究的主要针对工艺CPPs、质量控制CQAs、稳定性(含启甁稳定性)等进行了系统的研究,同时针对制剂体外溶出曲线与RLD进行了多种介质的比较,不同乙醇量的剂量倾泻实验以及添加不同表面活性剂的溶出曲线比较,结果显示仿制制剂体外溶出曲线与RLD高度拟合,最终通过BE,获得批准。
西安泰科迈医药在儿科、妇科、眼科、消化科、心脑血管、消化道、镇痛疾病的药品领域有深入的研究,在技术上专注于难溶、难吸收小分子药物制剂固体分散体开发、脂质体剂型开发、微球剂型开发、纳米晶剂型开发、增溶特殊辅料筛选和高浓蛋白药物制剂的蛋白喷雾干燥和蛋白结晶,在药物缓控释制剂、技术转化转移、工业化放大等领域有丰富的经验。以完善的管理体系和规范的工作流程为客户攻克技术难点,解决行业痛点。
西安泰科迈医药在项目研发中,精心系统设计、资源合理调配、计划任务时间精确、实施规范严格、鲁银药业配合密切是项目过关的保障。此项目的审核批准,是对西安泰科迈医药技术团队在原料药、创新药、仿制药、中药等技术开发中“科学严谨、精益求精、规范高效”原则的极大肯定,也诠释了质量源于设计的理念。
鲁银药业硝苯地平缓释片(Ⅱ)项目通过审批,是西安泰科迈医药为多个客户委托一致性评价研发品种通过审批后,再次通过仿制药一致性评价品种和客户,为团队积累和沉淀了逆向工程技术和管理经验。
愿我们泰科迈人用“严肃、严格、严谨”的态度不断提高业务能力、提升服务意识,不断追求技术与成本的卓越,迎接新的挑战、创造新的业绩。